| (C.14) |
La costante di equilibrio della reazione (C.2) e' legata ai potenziali standard delle due coppie redox dalla relazione (C.4):
| (C.14) |
Sostituendo i valori numerici
(
![]() ,
,
![]() ,
,
![]() ,
,
![]() ,
, ![]() ) si ricava
) si ricava
![]() . Cio'
significa che la reazione (C.2) e' virtualmente completa e
quindi si possono fare alcune ragionevoli approssimazioni.
. Cio'
significa che la reazione (C.2) e' virtualmente completa e
quindi si possono fare alcune ragionevoli approssimazioni.
Si puo' assumere
![]() . Allora, dalle
equazioni (C.11), (C.12) e (C.13) si
ricava facilmente:
. Allora, dalle
equazioni (C.11), (C.12) e (C.13) si
ricava facilmente:
e la curva puo' essere calcolata con l'equazione (C.7).
In questo caso, oltre alla equazione (C.11), deve valere anche:
Inoltre, per l'ipotesi di completezza della reazione (C.2), si ha:
Moltiplicando l'equazione (C.6) per 6, sommando ad essa l'equazione (C.5) e tenendo presenti le equazioni (C.11) (C.17) (C.18) si ottiene:
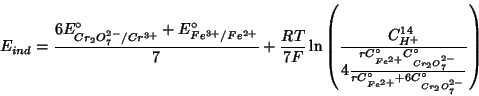
da cui si ricava la differenza di potenziale tramite l'equazione (C.1).
Si puo' assumere
![]() . Allora, dalle equazioni (C.11), (C.12) e (C.13) si
ricava facilmente:
. Allora, dalle equazioni (C.11), (C.12) e (C.13) si
ricava facilmente:
e la curva puo' essere calcolata con l'equazione (C.8).