



Next: Slide n. 67: il
Up: Slides delle lezioni del
Previous: Slide n. 65: il
- Siccome il numero di ossidazione di un atomo dipende dagli atomi
a cui esso si trova legato, un dato atomo puo' avere
diversi stati di ossidazione in diversi composti o addirittura atomi
identici aventi intorno chimico differente nella stessa molecola
possono avere numero di ossidazione differente
- Deve essere assolutamente chiaro che il numero di ossidazione
rappresenta una carica elettrica reale solo se l'elemento considerato
si trova come ione. Ad esempio
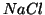 e' un vero e proprio composto
ionico che contiene i due ioni
e' un vero e proprio composto
ionico che contiene i due ioni 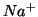 e
e 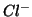 : ne segue
che il numero di ossidazione di
: ne segue
che il numero di ossidazione di 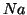 e
e 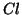 nel composto
nel composto 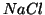 e'
e' 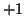 e
e 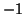 , rispettivamente.
, rispettivamente.
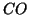 non e' un composto ionico (ad esempio, posto in acqua,
non si dissocia minimamente in ioni), tuttavia si trova che in questo
composto due degli elettroni dell'atomo di
non e' un composto ionico (ad esempio, posto in acqua,
non si dissocia minimamente in ioni), tuttavia si trova che in questo
composto due degli elettroni dell'atomo di 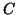 vengono attirati
verso l'atomo di
vengono attirati
verso l'atomo di 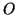 (che e' il piu' elettronegativo dei
due). Applicando la definizione di numero di ossidazione che abbiamo
dato, se i due elettroni dell'atomo di
(che e' il piu' elettronegativo dei
due). Applicando la definizione di numero di ossidazione che abbiamo
dato, se i due elettroni dell'atomo di 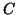 venissero (da notare
l'uso del condizionale) totalmente acquisiti dall'atomo di ossigeno,
allora quest'ultimo diventerebbe un anione con carica elettrica
venissero (da notare
l'uso del condizionale) totalmente acquisiti dall'atomo di ossigeno,
allora quest'ultimo diventerebbe un anione con carica elettrica
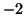 , mentre l'atomo di carbonio diventerebbe un catione con carica
elettrica
, mentre l'atomo di carbonio diventerebbe un catione con carica
elettrica 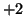 : si conclude che il numero di ossidazione di
: si conclude che il numero di ossidazione di 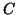 e
e
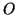 in
in 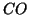 e'
e' 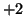 e
e 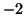 , rispettivamente
, rispettivamente
- In pratica il numero di ossidazione rende conto della
perturbazione che subiscono le nuvole elettroniche quando gli atomi si
legano per formare le molecole




Next: Slide n. 67: il
Up: Slides delle lezioni del
Previous: Slide n. 65: il