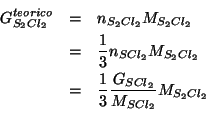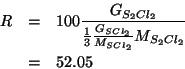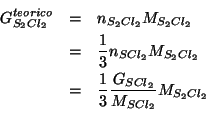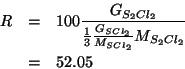Next: Slide n. 47: reazioni
Up: Slides delle lezioni del
Previous: Slide n. 45: una
- Resa di una reazione. Spesso la quantita' di prodotti che si
ottiene da una reazione e' inferiore a cio' che ci si potrebbe
aspettare dall'analisi della pura e semplice stechiometria (ad
esempio, una parte del prodotto puo' andare perduta durante i processi
di isolamento e purificazione). Si definisce resa percentuale
di una reazione la percentuale di prodotto ottenuto rispetto alla
quantita' teorica massima ottenibile.
Esempio 38
Il dicloruro di dizolfo si puo' ottenere dalla seguente reazione:
Se, partendo da una quantita'
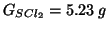 di
di 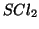 ed un eccesso
di
ed un eccesso
di 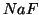 si ottengono
si ottengono
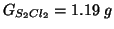 di
di 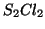 ,
qual'e' stata la resa percentuale della reazione?
Per trovare
,
qual'e' stata la resa percentuale della reazione?
Per trovare
 , tenendo presente che
, tenendo presente che
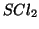 e' il reagente limitante:
Quindi:
e' il reagente limitante:
Quindi: