Next: Slide n. 439: esempio
Up: Slides delle lezioni del
Previous: Slide n. 437: elettrolisi
- La corrente che circola in una cella elettrochimica e' dovuta al
flusso degli elettroni prodotti o consumati in ciascuna semicella. Per
la legge di conservazione della carica prima vista, se in un certo
intervallo di tempo al catodo viene
prelevato un certo numero di moli di elettroni, all'anodo deve essere
ceduto lo stesso numero di moli di elettroni nello stesso intervallo
di tempo.
- La relazione quantitativa fra corrente e moli di sostanza
prodotte o consumate in una semicella e' data dalla stechiometria
della semireazione ad essa relativa. Infatti, la carica che attraversa
l'interfaccia elettrodica in un certo intervallo di tempo e' data
dalla relazione:
L'intensita' di corrente e il tempo sono grandezze misurabili molto
facilmente e con grande precisione.
- Nota la carica in Coulomb, la costante di Faraday consente di
trovare le moli di elettroni ad essa corrispondenti. Ricordiamo che la
costante di Faraday e' la carica elettrica in Coulomb corrispondente
ad una mole di elettroni. Quindi la costante di Faraday costituisce il
rapporto di equivalenza fra carica elettrica e moli di elettroni:
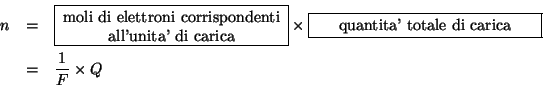
- Allora, data una quantita' di carica elettrica pari a
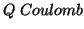 , le moli di elettroni
, le moli di elettroni 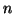 ad essa corrispondenti
saranno date da:
ad essa corrispondenti
saranno date da:
- Infine, dalla stechiometria della semireazione che avviene in
una semicella si puo' risalire facilmente al numero di moli di
reagenti consumati o a quello di prodotti formati in seguito
all'elettrolisi.




Next: Slide n. 439: esempio
Up: Slides delle lezioni del
Previous: Slide n. 437: elettrolisi