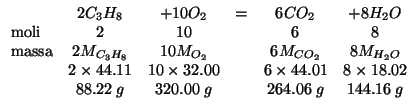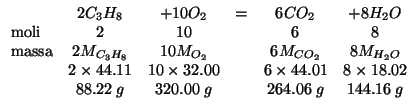Next: Slide n. 43: esempi
Up: Slides delle lezioni del
Previous: Slide n. 41: eventi
- I rapporti in moli espressi da un'equazione chimica bilanciata
possono essere trasformati immediatamente in rapporti in massa
utilizzando la definizione di massa molare
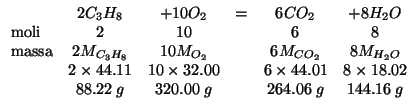
- Reagente limitante. Se i reagenti di una reazione chimica vengono
posti a reagire in rapporto quantitativo esattamente uguale a quello
dettato dalla stechiometria, allora, ammesso che la reazione proceda
indefinitamente (``reazione completa''), tutti verranno
consumati completamente. Tuttavia, se il rapporto quantitativo fra i
reagenti e' diverso da quello stechiometrico, allora
necessariamente uno di essi sara' in difetto rispetto alla
quantita' stechiometricamente necessaria: la reazione
procedera' fino a che sara' presente il reagente in difetto, ma quando
tutto tale reagente sara' stato consumato, la reazione non potra' procedere
oltre, anche se sono ancora presenti gli altri reagenti. Il reagente in
difetto viene chiamato reagente limitante, perche' e' esso che
limita il massimo grado di avanzamento possibile della reazione.
- Da sottolineare: il concetto di reagente limitante vale solo per
le reazioni complete, cioe' quelle che procedono indefinitamente fino a
che ci sono reagenti da convertire. Vedremo che non tutte (anzi solo
poche) reazioni sono complete: moltissime reazioni (le reazioni ``di
equilibrio'') non arrivano a consumare completamente nessuno dei reagenti




Next: Slide n. 43: esempi
Up: Slides delle lezioni del
Previous: Slide n. 41: eventi