



Next: Slide n. 383: il
Up: Slides delle lezioni del
Previous: Slide n. 381: il
- L'applicazione del secondo principio per decidere se un processo
e' spontaneo o meno e' scomoda per il fatto che richiede la
determinazione di
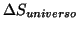 . Sarebbe molto utile un
criterio che coinvolga il solo sistema.
. Sarebbe molto utile un
criterio che coinvolga il solo sistema.
- A questo scopo esiste una funzione di stato detta
energia libera di Gibbs. Per un processo che avvenga a
temperatura e pressione costante, la variazione dell'energia libera di
Gibbs e' data da:
dove tutte le variazioni delle funzioni di stato al secondo membro si
riferiscono al solo sistema
- Il secondo principio puo' essere espresso in termini di energia
libera di Gibbs. Per un processo isotermo (temperatura costante) e
isobaro (pressione costante), il criterio di spontaneita' e':
- Il passaggio:
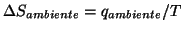 e' lecito
solo se lo scambio di calore avviene in modo reversibile. In effetti,
l'ambiente si comporta come ``un serbatoio di calore infinito'', e
quindi lo scambio di calore comporta per l'ambiente un discostamento
solo infinitesimo dalla condizione di equilibrio, il che implica la
reversibilita' richiesta.
e' lecito
solo se lo scambio di calore avviene in modo reversibile. In effetti,
l'ambiente si comporta come ``un serbatoio di calore infinito'', e
quindi lo scambio di calore comporta per l'ambiente un discostamento
solo infinitesimo dalla condizione di equilibrio, il che implica la
reversibilita' richiesta.
- Si vede quindi che, per processi che avvengano in condizioni di
temperatura e pressione costanti, che sono condizioni estremamente
comuni, si ha:




Next: Slide n. 383: il
Up: Slides delle lezioni del
Previous: Slide n. 381: il

