



Next: Slide n. 376: reazione
Up: Slides delle lezioni del
Previous: Slide n. 374: l'entropia
- L'interpretazione dell'entropia come ``grado di disordine di un
sistema'' e' utile da un punto di vista qualitativo. Per poter dare
una definizione quantitativa di entropia bisogna prima introdurre il
concetto di reversibilita' termodinamica.
- Si definisce termodinamicamente reversibile un processo in cui
il sistema si trova sempre in condizioni infinitamente vicine all'equilibrio
- In pratica, un processo reversibile e' inattuabile; tuttavia un
processo puo' essere fatto avvenire in condizioni vicine a piacere
alla reversibilita'.
- Esempio.
L'espansione di un gas ideale puo' essere fatta
avvenire in condizioni reversibili nel modo seguente. Supponiamo che
il gas si trovi in un cilindro con pistone; allora, se lo si vuole
espandere dal volume iniziale 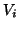 a quello finale
a quello finale 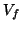 in modo
reversibile, bastera' sollevare il pistone molto lentamente. Durante
il sollevamento del pistone, la pressione esercitata dal gas
differisce di pochissimo da quella esercitata dal pistone sul
gas e quindi il gas, pur compiendo l'espansione, si trova sempre in
condizioni vicinissime all'equilibrio.
in modo
reversibile, bastera' sollevare il pistone molto lentamente. Durante
il sollevamento del pistone, la pressione esercitata dal gas
differisce di pochissimo da quella esercitata dal pistone sul
gas e quindi il gas, pur compiendo l'espansione, si trova sempre in
condizioni vicinissime all'equilibrio.
- E' da notare la differenza rispetto al caso in cui il pistone
viene alzato improvvisamente e portato al volume finale: lo
stato finale e' esattamente lo stesso, ma durante la trasformazione il
gas e' ben lontano da una qualsiasi condizione di equilibrio: la
pressione esercitata dal gas sul pistone e' uguale a quella
nel caso precedente, ma la pressione esercitata dal pistone
sul gas durante l'espansione e' praticamente nulla




Next: Slide n. 376: reazione
Up: Slides delle lezioni del
Previous: Slide n. 374: l'entropia