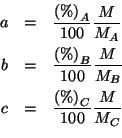
si puo' fare il rapporto membro a membro delle equazioni per eliminare
la massa molare ![]() e ricavare i rapporti in cui sono combinati gli
elementi che costituiscono la molecola:
e ricavare i rapporti in cui sono combinati gli
elementi che costituiscono la molecola:
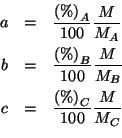
si puo' fare il rapporto membro a membro delle equazioni per eliminare
la massa molare ![]() e ricavare i rapporti in cui sono combinati gli
elementi che costituiscono la molecola:
e ricavare i rapporti in cui sono combinati gli
elementi che costituiscono la molecola: