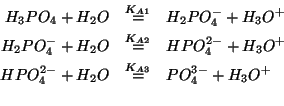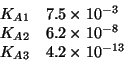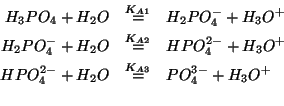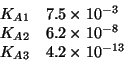Next: Slide n. 318: idrolisi
Up: Slides delle lezioni del
Previous: Slide n. 316: base
Acidi poliprotici.
- Come abbiamo gia' visto, molti acidi possono cedere piu' di un
protone (ad esempio
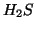 ,
, 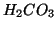 ,
, 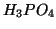 ,
,
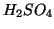 ).
).
- Ad ogni protone ceduto, corrisponde un equilibrio di
ionizzazione, caratterizzato da una costante di equilibrio:
- Per un acido poliprotico, le costanti di equilibrio di
ionizzazioni successive sono sempre piu' piccole. Ad esempio, per
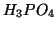 si ha:
si ha:
- Il motivo di quanto sopra e' facilmente spiegabile con semplici
argomenti di tipo elettrostatico: l'allontanamento di un protone
(carico positivamente) da una certa specie chimica sara' tanto piu'
difficile quanto maggiore e' la carica negativa della specie chimica.
- Il calcolo rigoroso del
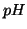 in una soluzione acquosa di un
acido poliprotico e' complicato dal fatto che la concentrazione di
ioni idronio in soluzione e' dovuta a tutti i possibili stadi di
ionizzazione dell'acido.
in una soluzione acquosa di un
acido poliprotico e' complicato dal fatto che la concentrazione di
ioni idronio in soluzione e' dovuta a tutti i possibili stadi di
ionizzazione dell'acido.
- Tuttavia, molto spesso, le costanti di ionizzazione successive
alla prima sono molto piu' piccole e cio' fa si' che il calcolo del
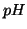 possa essere basato, almeno in prima approssimazione, solo sul
primo stadio di ionizzazione.
possa essere basato, almeno in prima approssimazione, solo sul
primo stadio di ionizzazione.




Next: Slide n. 318: idrolisi
Up: Slides delle lezioni del
Previous: Slide n. 316: base