Alcune specie chimiche (dette anfiprotiche) possono sia cedere che acquistare un protone: esse si comportano quindi sia da acidi che da basi di Lowry e Brönsted
oppure da acido, cedendo un protone ad una base e trasformandosi in ione ossidrile:
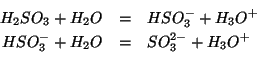
Lo ione idrogeno solfito,