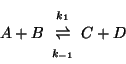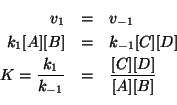Next: Slide n. 280: calcoli
Up: Slides delle lezioni del
Previous: Slide n. 278: spiegazione
- Influenza della temperatura.
Variazioni di concentrazione o di pressione spostano un equilibrio in
un senso o nell'altro, ma non alterano il valore della costante di
equilibrio. Una variazione di temperatura, invece, produce un
cambiamento del valore della costante di equilibrio.
- La dipendenza della costante di equilibrio dalla temperatura
puo' essere razionalizzata in modo qualitativo per il caso particolare
di una reazione elementare bimolecolare:
Si e' visto che, per questo caso particolare, la costante di
equilibrio e' in relazione con le costanti cinetiche della reazione
diretta e di quella inversa:
- Una variazione di temperatura provoca un cambiamento delle due
costanti cinetiche (che dipendono dalla temperatura tramite
l'equazione di Arrhenius): siccome le costanti cinetiche cambiano in
modo diverso, anche il loro rapporto (e quindi la costante di
equilibrio) cambia con la temperatura.
- La variazione della costante di equilibrio con la temperatura
puo' essere predetta sulla base del principio di Le Chatelier: se una
reazione e' endotermica, un aumento di temperatura (cioe'
un'immissione di calore nel sistema) deve favorire la formazione dei
prodotti, cioe' deve provocare un aumento della costante di
equilibrio.
- In modo analogo si comprende che, per una reazione esotermica,
un aumento di temperatura provoca una diminuzione della costante di
equilibrio.




Next: Slide n. 280: calcoli
Up: Slides delle lezioni del
Previous: Slide n. 278: spiegazione