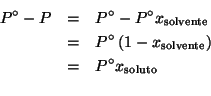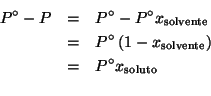Next: Slide n. 228: innalzamento
Up: Slides delle lezioni del
Previous: Slide n. 226: le
- Siccome la frazione molare del solvente e' sempre un numero
minore dell'unita', segue che la presenza di un soluto non volatile
diminuisce la pressione di vapore del solvente ad ogni temperatura.
- L'abbassamento della pressione di vapore di una soluzione e' una
tipica proprieta' colligativa e, nel caso di comportamento ideale,
puo' essere messo facilmente in relazione con la frazione molare del
soluto:
- L'interpretazione molecolare dell'abbassamento della pressione
di vapore causato da un soluto non volatile e' abbastanza semplice,
almeno su un piano qualitativo: la presenza del soluto fa si che la
concentrazione di molecole di solvente alla superficie della soluzione
sia minore di quella del solvente puro e cio' implica una
diminuzione della velocita' di evaporazione ad una data
temperatura. Siccome l'equilibrio viene raggiunto quando la velocita'
di condensazione eguaglia quella di evaporazione, e siccome la
velocita' di condensazione e' proporzionale alla pressione del vapore,
segue che l'equilibrio si instaura ad una pressione di vapore
inferiore a quella necessaria nel solvente puro.