



Next: Slide n. 218: la
Up: Slides delle lezioni del
Previous: Slide n. 216: applicazione
Diagrammi di fase.
- Riconsideriamo l'esperimento dell'equilibrio liquido
vapore. Abbiamo visto che, per ogni temperatura del bagno
termostatico, si raggiunge una (e una soltanto) determinata pressione
di equilibrio. Possiamo allora eseguire una serie di misure della
pressione di equilibrio corrispondente a temperature via via minori a
partire, ad esempio, dalla temperatura ambiente. Riportando le coppie
di valori
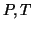 cosi' ottenuti in un grafico otterremo un ramo di
curva che rappresenta il luogo dei punti in cui acqua liquida e acqua
vapore coesistono in equilibrio (figura).
cosi' ottenuti in un grafico otterremo un ramo di
curva che rappresenta il luogo dei punti in cui acqua liquida e acqua
vapore coesistono in equilibrio (figura).
- Continuando a diminuire la temperatura del termostato, si
arrivera' al punto in cui l'acqua appena introdotta ghiaccia. Anche in
questo caso, tuttavia, parte dell'acqua solida evaporera' per occupare
il volume vuoto a disposizione generando una pressione di equilibrio
con un meccanismo perfettamente analogo a quello che abbiamo discusso
per l'equilibrio liquido vapore.
- Continuando ad eseguire misure a temperatura sempre piu' bassa,
possiamo tracciare sul diagramma
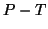 un secondo ramo
di curva che rappresenta il luogo dei punti in cui acqua solida e
acqua vapore coesistono in equilibrio (figura)
un secondo ramo
di curva che rappresenta il luogo dei punti in cui acqua solida e
acqua vapore coesistono in equilibrio (figura)
- Chiaramente questo secondo ramo di curva si ottiene come
continuazione del primo (semplicemente, a un certo punto, l'acqua
introdotta nel recipiente non resta piu' liquida, ma diventa
ghiaccio): ne segue che, nel corso della diminuzione di temperatura,
dobbiamo essere passati per una coppia di valori
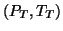 in cui si ha coesistenza di acqua liquida,
solida e gassosa in condizioni di equilibrio (figura). Tale punto nel
piano
in cui si ha coesistenza di acqua liquida,
solida e gassosa in condizioni di equilibrio (figura). Tale punto nel
piano 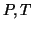 viene detto punto triplo.
viene detto punto triplo.




Next: Slide n. 218: la
Up: Slides delle lezioni del
Previous: Slide n. 216: applicazione