



Next: Slide n. 201: forze
Up: Slides delle lezioni del
Previous: Slide n. 199: legame
- Forze dipolo-dipolo indotto.
Una molecola polare puo' indurre un momento di dipolo in una molecola
apolare.
Ad esempio, se una molecola di ossigeno si avvicina ad una molecola di
acqua orientata verso di essa con l'atomo di ossigeno, la frazione di
carica negativa presente su quest'ultimo respinge la nuvola
elettronica della molecola di ossigeno e attira la carica positiva
nucleare. Cio' determina uno spostamento del baricentro della carica
negativa rispetto a quello della carica positiva nella molecola di
ossigeno e quindi induce una polarita'.
- La molecola di ossigeno polarizzata interagisce con la molecola
di acqua polare come abbiamo gia' descritto parlando delle interazioni
dipolo-dipolo.
- Le interazioni dipolo-dipolo indotto sono generalmente piu'
deboli di quelle dipolo-dipolo, tuttavia, ad esempio, e' grazie ad
esse che molti gas apolari (come
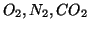 ) mostrano una
discreta solubilita' in acqua.
) mostrano una
discreta solubilita' in acqua.
- La tendenza di un atomo, ione o molecola a manifestare una
polarita' per induzione si chiama polarizzabilita'.
- Siccome l'induzione di un momento di dipolo dipende dalla
facilita' con cui la nuvola elettronica viene deformata, e' logico
aspettarsi che la polarizzabilita' aumenti all'aumentare delle
dimensioni atomiche o molecolari. Infatti, quanto piu' gli elettroni
sono distanti dal nucleo, tanto meno fortemente sono trattenuti da
quest'ultimo e quindi tanto piu' facile sara' il loro spostamento
sotto l'effetto di un campo elettrico.
- Anche uno ione puo' indurre un dipolo in una specie apolare con
lo stesso meccanismo visto sopra.




Next: Slide n. 201: forze
Up: Slides delle lezioni del
Previous: Slide n. 199: legame