E' un tipo di interazione dipolo-dipolo particolarmente intensa e si verifica quando un atomo di idrogeno, legato ad un atomo molto piu' elettronegativo, interagisce con una coppia solitaria di un altro atomo di questo tipo.
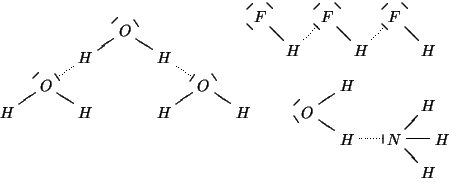
Ad esempio, a causa del legame idrogeno, il punto di ebollizione dell'acqua (