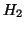- L'inerzia chimica dei gas nobili (ampiamente verificata sperimentalmente) suggerisce che questi elementi si trovino in una situazione elettronica particolarmente stabile e gli atomi degli altri elementi si combinano tra loro condividendo coppie di elettroni per raggiungere lo stesso tipo di stabilita'
- Tutti i gas nobili, tranne l'elio, hanno una configurazione
elettronica con otto elettroni nello strato di valenza: gli atomi degli
altri elementi tendono a condividere coppie elettroniche in modo da
raggiungere la stessa configurazione del gas nobile piu' vicino
(configurazione ad ottetto, tranne
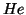 , che ha una
configurazione stabile a due elettroni, guscio
, che ha una
configurazione stabile a due elettroni, guscio 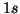 completo)
completo)
- Dato che gli elettroni di valenza di un atomo sono quelli meno fortemente legati, e' naturale che solo tali elettroni vengano coinvolti nella formazione dei legami, mentre gli elettroni piu' interni non risentono dell'avvicinamento di altri atomi
Esempio 45
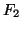 ,
, 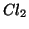 ,
, 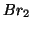 ,
,