



Next: Slide n. 127: le
Up: Slides delle lezioni del
Previous: Slide n. 125: la
Il legame ionico
- Si parla di legame ionico per composti costituiti da ioni: tali
ioni sono legati da forze di attrazione elettrostatica e derivano dal
trasferimento di elettroni da atomi con bassa energia di ionizzazione ad
atomi con elevata affinita' elettronica
- Questo spiega come mai la maggior parte dei composti ionici sia
formata da cationi metallici (parte sinistra della tavola periodica,
bassa energia di ionizzazione) combinati con anioni di non metalli
(parte destra della tavola periodica, elevata affinita' elettronica)
- I composti ionici allo stato solido formano un reticolo
cristallino ordinato tridimensionale in cui ogni catione risente
dell'attrazione elettrostatica di diversi anioni, e viceversa
Esempio 44
La struttura di 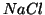 e' costituita dalla compenetrazione di due
sub-reticoli a facce centrate di ioni
e' costituita dalla compenetrazione di due
sub-reticoli a facce centrate di ioni 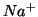 e
e 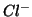 .
.
- Una misura diretta della forza di un legame ionico e' l'energia di
dissociazione di una coppia di ioni allo stato gassoso, definita come
variazione di energia per il processo:
La forza del legame ionico tra 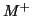 ed
ed 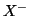 e' tanto maggiore
quanto maggiore e' il valore (determinabile sperimentalmente) di
e' tanto maggiore
quanto maggiore e' il valore (determinabile sperimentalmente) di
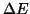 .
.
- Una previsione qualitativa di
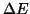 puo' essere fatta
tenendo presente l'espressione della forza di Coulomb:
puo' essere fatta
tenendo presente l'espressione della forza di Coulomb:
C'e' da aspettarsi che il legame ionico sia piu' forte (e quindi che
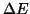 sia maggiore) per composti formati da piccoli ioni di
carica elevata. Ad esempio:
sia maggiore) per composti formati da piccoli ioni di
carica elevata. Ad esempio:
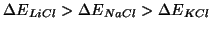 e
e
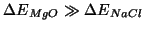 .
.




Next: Slide n. 127: le
Up: Slides delle lezioni del
Previous: Slide n. 125: la
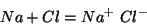
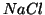 e' costituita dalla compenetrazione di due
sub-reticoli a facce centrate di ioni
e' costituita dalla compenetrazione di due
sub-reticoli a facce centrate di ioni 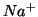 e
e 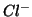 .
.