Un recipiente da ![]() chiuso e collegato ad un manometro
contiene bicromato d'ammonio ad una temperatura di
chiuso e collegato ad un manometro
contiene bicromato d'ammonio ad una temperatura di ![]() . Si
riscalda ad alta temperatura favorendo la seguente reazione di
decomposizione:
. Si
riscalda ad alta temperatura favorendo la seguente reazione di
decomposizione:
![]()
Si lascia raffreddare a ![]() . La pressione finale e' salita da
. La pressione finale e' salita da
![]() a
a ![]() . Calcolare quanti grammi di
. Calcolare quanti grammi di ![]() \
si sono formati.
\
si sono formati.
La tensione di vapore dell'acqua a ![]() e' di
e' di ![]() .
.
SVOLGIMENTO
Dati:
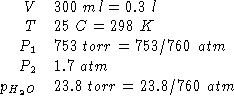
Altri simboli:
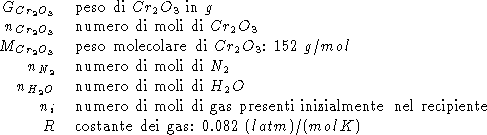
![]()
Per trovare ![]() :
:
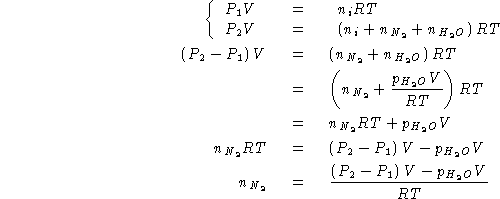
Sostituendo nella (1):
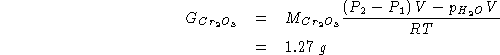
Si dispone di una soluzione ![]() di
di ![]() e di una
soluzione
e di una
soluzione ![]() di
di ![]() . Calcolare i volumi delle due
soluzioni che, mescolate, servono a preparare un litro di tampone
. Calcolare i volumi delle due
soluzioni che, mescolate, servono a preparare un litro di tampone
![]() che abbia pH=7.35.
che abbia pH=7.35.
Nella soluzione tampone e' presente il seguente equilibrio:
![]()
( ![]() ).
).
SVOLGIMENTO
Dati:
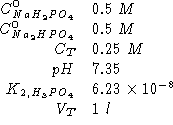
Altri simboli:

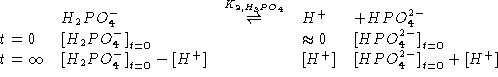
![]()
NOTA:
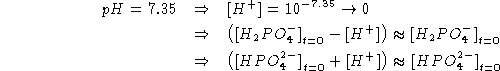
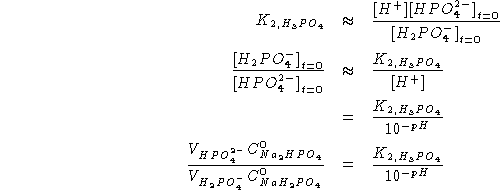
Il vincolo soprastante deve essere verificato da
![]() e
e ![]() \
insieme al vincolo sulla concentrazione del tampone e a quello sul
volume totale:
\
insieme al vincolo sulla concentrazione del tampone e a quello sul
volume totale:
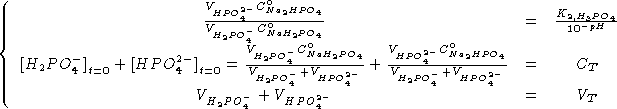
NOTA: il sistema su scritto e' ridondante (): si deve aggiungere un volume di acqua come terza incognita
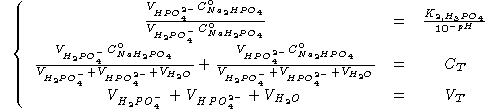
Moltiplicando la seconda equazione per la terza:
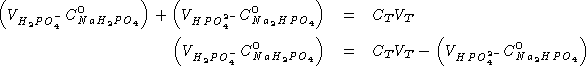
Sostituendo nella prima:
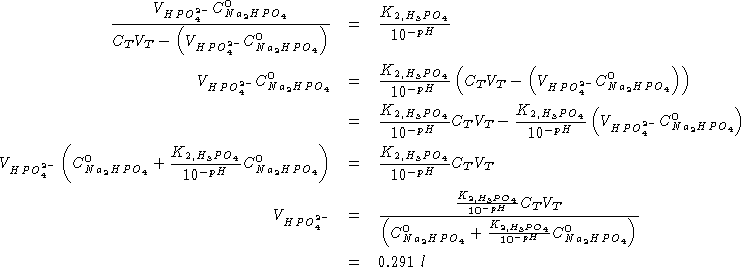
Sostituendo a ritroso:
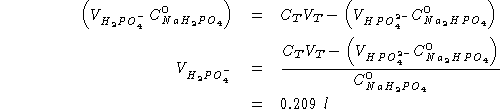
Infine, dalla terza equazione del sistema:
![]()
Dopo aver bilanciato in forma molecolare la seguente reazione:
![]()
calcolare quanto perclorato di sodio si ottiene facendo reagire, in
base all'equazione bilanciata, ![]() di fluoro gassoso, misurati
a
di fluoro gassoso, misurati
a ![]() e
e ![]() , con
, con ![]() di una soluzione
di una soluzione ![]() \
di idrossido di sodio avente densita'
\
di idrossido di sodio avente densita' ![]() .
.
SVOLGIMENTO
Dati:
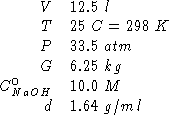
Altri simboli:

NOTA: Sia Mn che Cl insi ossidano
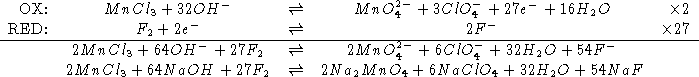
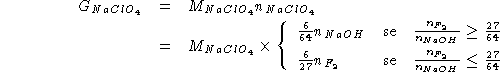
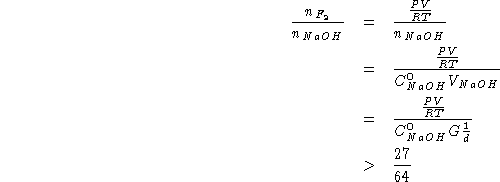
Quindi:
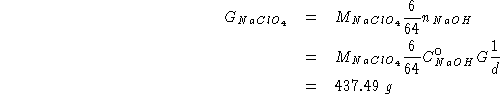
Un litro di una soluzione ![]() di KCN trattato
con un eccesso di AgI, ne sciglie
di KCN trattato
con un eccesso di AgI, ne sciglie ![]() . Calcolare la costante
di formazione dello ione complesso
. Calcolare la costante
di formazione dello ione complesso ![]() che si ottiene
dalla reazione:
che si ottiene
dalla reazione:
![]()
sapendo che il prodotto di solubilita' di AgI e' di
![]() .
.
SVOLGIMENTO
Dati:
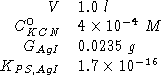
Altri simboli:

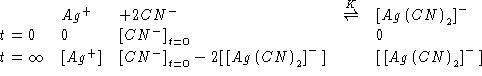
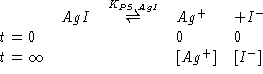
Dalla (2):

Sostituendo nella (3):
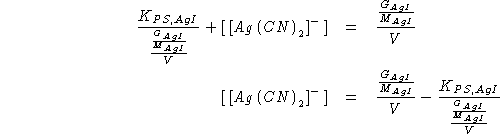
Infine, sostituendo nella (1):
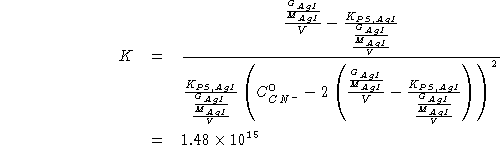
Una miscela formata da ![]() di HCl e da
di HCl e da ![]() di
di
![]() viene posta a reagire a
viene posta a reagire a ![]() ed
ed
![]() . All'equilibrio si sono formate
. All'equilibrio si sono formate ![]() di
di
![]() . Si richiedono le costanti
. Si richiedono le costanti ![]() ,
, ![]() e
e ![]() \
della reazione:
\
della reazione:
![]()
SVOLGIMENTO
Dati:
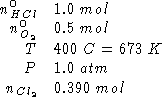
Altri simboli:

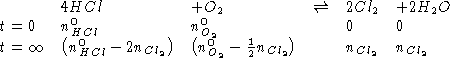
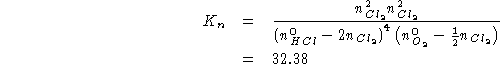
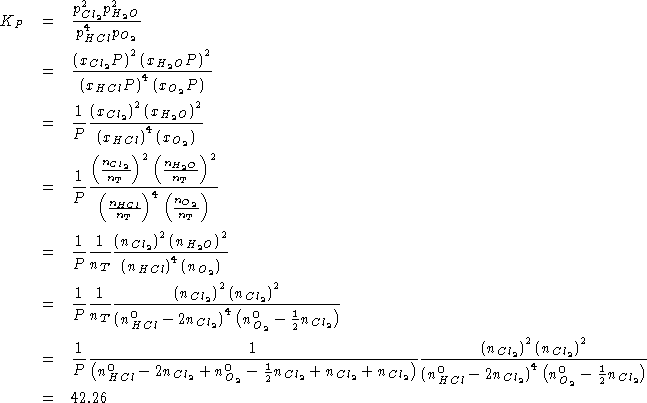
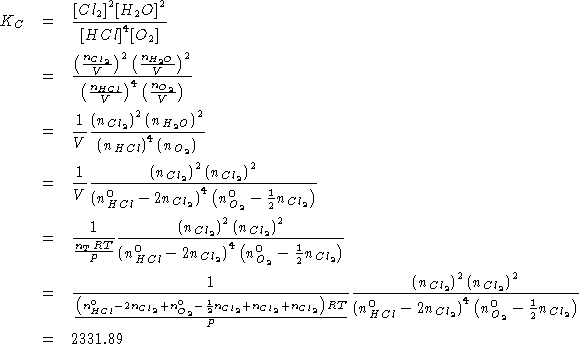
%