![\begin{psfrags}\psfrag{dummy}{}\psfrag{voltmeter} [c][c]{strumento di misur...
...$}}\psfrag{Cl} [l][l]{{$Cl^-$}}
\includegraphics{single-pot.eps}
\end{psfrags}](img143.gif)
Da quanto detto finora, sembrerebbe logico poter realizzare una titolazione potenziometrica trasformando il beaker contenente la soluzione da titolare in una semicella.
![\begin{psfrags}\psfrag{dummy}{}\psfrag{voltmeter} [c][c]{strumento di misur...
...$}}\psfrag{Cl} [l][l]{{$Cl^-$}}
\includegraphics{single-pot.eps}
\end{psfrags}](img143.gif)
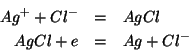
#!@acc..dann..malediz..#!@: un singolo potenziale elettrodico non si puo' misurare!!!