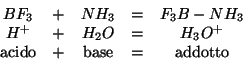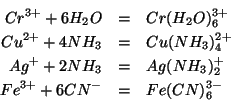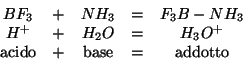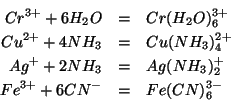Next: Slide n. 359: idrolisi
Up: Slides delle lezioni del
Previous: Slide n. 357: acidi
- La specie chimica che si origina in seguito alla formazione del
legame dativo fra una base (donatore della coppia elettronica) e un
acido di Lewis (accettore della coppia elettronica) viene detta
complesso o addotto acido base.
- Molti cationi metallici si comportano da acidi di Lewis, formando
legami donatore/accettore con molecole d'acqua o altre molecole o ioni
in grado di comportarsi da donatori di coppie elettroniche:
- Queste reazioni di formazione di addotti acido base sono
caratterizzate da costanti di equilibrio che vengono spesso dette
costanti di formazione.
- La reazione di formazione di addotti acido base fra cationi
metallici e molecole di acqua e' la gia' citata reazione di
idratazione. Questa reazione spiega come mai i sali di molti cationi
metallici danno un idrolisi acida. Infatti, la coordinazione dell'acqua
allo ione metallico positivo produce un impoverimento elettronico
dell'ossigeno e quindi induce una piu' facile rottura di un legame
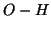 , come e' stato gia' sottolineato in precedenza
, come e' stato gia' sottolineato in precedenza




Next: Slide n. 359: idrolisi
Up: Slides delle lezioni del
Previous: Slide n. 357: acidi