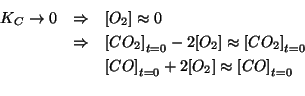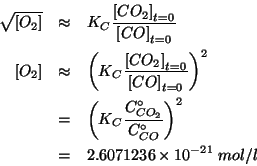Next: Slide n. 298: segue
Up: Slides delle lezioni del
Previous: Slide n. 296: segue
In modo analogo a quanto visto per il caso
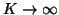 , si
puo' procedere in modo alternativo impostando il trattamento generale
dell'equilibrio ed introducendo le semplificazioni derivanti dal
valore molto piccolo della costante di equilibrio a livello della
legge dell'azione di massa. Scegliendo come incognita la
concentrazione di equilibrio di
, si
puo' procedere in modo alternativo impostando il trattamento generale
dell'equilibrio ed introducendo le semplificazioni derivanti dal
valore molto piccolo della costante di equilibrio a livello della
legge dell'azione di massa. Scegliendo come incognita la
concentrazione di equilibrio di 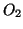 :
:
La legge dell'azione di massa si scrive come:
A questo punto si sfrutta il fatto che la costante di equilibrio e'
molto piccola: come gia' detto, cio' implica che la quantita' di
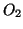 formata sara' molto piccola e quindi trascurabile rispetto
alle concentrazioni iniziali degli altri due partecipanti. In modo
conciso:
formata sara' molto piccola e quindi trascurabile rispetto
alle concentrazioni iniziali degli altri due partecipanti. In modo
conciso:
Quindi la legge dell'azione di massa puo' essere semplificata in:
Anche in questo caso non si puo' sostituire 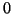 al posto di
al posto di
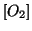 al numeratore, altrimenti l'espressione perde
significato.
al numeratore, altrimenti l'espressione perde
significato.
A questo punto:
Ovviamente, il risultato e' identico a quello ottenuto con
l'impostazione precedente.




Next: Slide n. 298: segue
Up: Slides delle lezioni del
Previous: Slide n. 296: segue
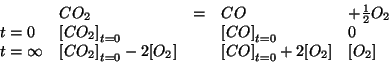
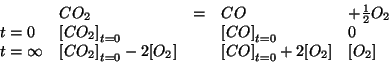
![]() formata sara' molto piccola e quindi trascurabile rispetto
alle concentrazioni iniziali degli altri due partecipanti. In modo
conciso:
formata sara' molto piccola e quindi trascurabile rispetto
alle concentrazioni iniziali degli altri due partecipanti. In modo
conciso: