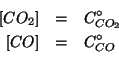La costante di equilibrio per la reazione:
e'
In questo caso, non ci sono dubbi sulla direzione in cui evolvera' la
reazione per raggiungere l'equilibrio: siccome la concentrazione
iniziale di ![]() e' nulla, il quoziente di reazione iniziale vale
e' nulla, il quoziente di reazione iniziale vale
![]() e quindi la reazione si spostera' verso destra per formare un
po' di
e quindi la reazione si spostera' verso destra per formare un
po' di ![]() e far quindi aumentare il quoziente di
reazione fino al valore prescritto dalla costante di equilibrio.
e far quindi aumentare il quoziente di
reazione fino al valore prescritto dalla costante di equilibrio.
Appurata la direzione in cui si evolve la reazione, possiamo sfruttare
il fatto che
![]() . In pratica, questo significa che la
reazione si sposta si' verso destra, ma di molto poco. In altre
parole, possiamo dire che e' sufficiente che si formi una quantita'
piccolissima di
. In pratica, questo significa che la
reazione si sposta si' verso destra, ma di molto poco. In altre
parole, possiamo dire che e' sufficiente che si formi una quantita'
piccolissima di ![]() affinche' il quoziente di reazione diventi
uguale alla costante di equilibrio. Se assumiamo che si formi una
quantita' trascurabilmente piccola di
affinche' il quoziente di reazione diventi
uguale alla costante di equilibrio. Se assumiamo che si formi una
quantita' trascurabilmente piccola di ![]() , possiamo altresi'
assumere che le concentrazioni di equilibrio di
, possiamo altresi'
assumere che le concentrazioni di equilibrio di ![]() e
e ![]() rimangano praticamente inalterate:
rimangano praticamente inalterate: