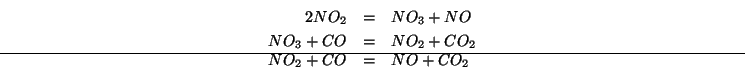Esempio 59
La reazione:
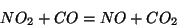
non avviene in seguito ad un unico urto fra una molecola di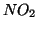 ed una di
ed una di 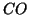 . Invece, il meccanismo della reazione e' costituito
da due stadi elementari:
. Invece, il meccanismo della reazione e' costituito
da due stadi elementari:
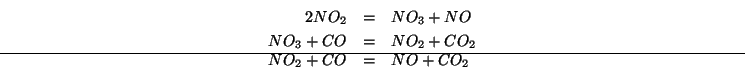
non avviene in seguito ad un unico urto fra una molecola di