



Next: Slide n. 247: orientazione;
Up: Slides delle lezioni del
Previous: Slide n. 245: figura
- Oltrepassato il massimo, l'energia del sistema decresce
all'aumentare della coordinata di reazione: il legame
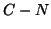 finisce di spezzarsi, quello
finisce di spezzarsi, quello 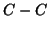 finisce di formarsi e il gruppo
finisce di formarsi e il gruppo
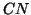 si dispone nell'orientazione che ha nell'acetonitrile. Infine,
l'energia raggiunge il valore corrispondente al prodotto di reazione,
cioe' l'acetonitrile.
si dispone nell'orientazione che ha nell'acetonitrile. Infine,
l'energia raggiunge il valore corrispondente al prodotto di reazione,
cioe' l'acetonitrile.
- Nella trasformazione ad acetonitrile, l'isocianuro di metile
deve superare una barriera energetica il cui valore e' dato dalla
differenza fra il massimo del profilo di reazione e l'energia dello
stato iniziale. Tale barriera si chiama energia di
attivazione.
- Dunque, esiste un valore minimo di energia che una molecola deve
possedere per poter reagire: solo le molecole che possiedono
un'energia maggiore all'energia di attivazione potranno portare al
prodotto, anche se l'energia di quest'ultimo e' minore di quella del
reagente di partenza (come ad esempio nel caso della trasformazione
dell'isocianuro in acetonitrile)
- L'energia necessaria al superamento della barriera di
attivazione proviene dagli urti fra le molecole: quando due molecole
di isocianuro si urtano, si ha un trasferimento di energia che puo'
consentire ad una delle due il superamento della barriera di attivazione.
- L'energia trasferita in un urto fra due molecole dipende
dall'energia cinetica posseduta dalle molecole che si urtano e questa
dipende direttamente dalla temperatura: all'aumentare della
temperatura, aumenta la frazione di molecole che si urtano con energia
sufficiente al superamento della barriera di attivazione. In generale,
dunque, ci si aspetta un aumento della velocita' di reazione
all'aumentare della temperatura.




Next: Slide n. 247: orientazione;
Up: Slides delle lezioni del
Previous: Slide n. 245: figura