



Next: Slide n. 240: determinazione
Up: Slides delle lezioni del
Previous: Slide n. 238: segue
- La velocita' di una reazione dipende dalla concentrazione e
dalla temperatura.
- Per molte reazioni, si trova sperimentalmente che la velocita'
di reazione dipende in modo semplice dalla concentrazione dei
reagenti. Ad esempio, per la generica reazione:
si trova spesso che la velocita' di reazione e' data da
- La relazione che lega la velocita' di una reazione alla
concentrazione dei reagenti viene detta legge cinetica. La
legge cinetica per una reazione puo' essere determinata solo
per via sperimentale.
- Nei casi piu' semplici, la legge cinetica contiene le concentrazioni
dei reagenti, ciascuna elevata ad un esponente, che viene detto
ordine di reazione. Nell'esempio visto sopra,
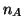 e'
l'ordine di reazione rispetto al reagente
e'
l'ordine di reazione rispetto al reagente 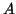 ,
, 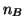 e' l'ordine
di reazione rispetto al reagente
e' l'ordine
di reazione rispetto al reagente 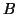 e cosi' via. La somma degli ordini di
reazione si dice ordine di reazione complessivo. Nell'esempio
l'ordine di reazione complessivo e'
e cosi' via. La somma degli ordini di
reazione si dice ordine di reazione complessivo. Nell'esempio
l'ordine di reazione complessivo e'
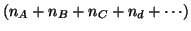 .
.
- In generale, l'ordine di reazione rispetto ad un reagente non ha
alcuna relazione con il suo coefficiente stechiometrico. Ad esempio,
per la reazione:
si trova sperimentalmente che la velocita' di reazione e' data dalla
seguente legge cinetica:
L'ordine di reazione rispetto a 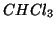 e'
e' 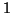 come il suo
coefficiente stechiometrico, ma l'ordine di reazione rispetto a
come il suo
coefficiente stechiometrico, ma l'ordine di reazione rispetto a
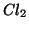 e'
e' 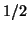 mentre il suo coefficiente stechiometrico e'
mentre il suo coefficiente stechiometrico e' 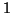 .
.
- La costante
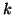 che compare nella legge cinetica si chiama
costante cinetica e non dipende dalle concentrazioni. Essa
tuttavia dipende dalla temperatura e percio' determina la dipendenza
della velocita' di reazione dalla temperatura.
che compare nella legge cinetica si chiama
costante cinetica e non dipende dalle concentrazioni. Essa
tuttavia dipende dalla temperatura e percio' determina la dipendenza
della velocita' di reazione dalla temperatura.




Next: Slide n. 240: determinazione
Up: Slides delle lezioni del
Previous: Slide n. 238: segue