



Next: Slide n. 235: massa
Up: Slides delle lezioni del
Previous: Slide n. 233: la
L'effetto della dissociazione elettrolitica sulle proprieta'
colligative.
- Si e' detto che le proprieta' colligative (abbassamento della
pressione di vapore, innalzamento ebullioscopico, abbassamento
crioscopico e pressione osmotica) dipendono dalla concentrazione
totale di particelle di soluto in soluzione.
- Questo significa che nel calcolo della concentrazione di soluto
bisogna tenere conto del suo eventuale comportamento dissociativo.
- Ad esempio,
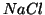 e' un elettrolita forte e quindi una
soluzione
e' un elettrolita forte e quindi una
soluzione 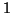 molale di
molale di 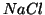 contiene in realta' una
concentrazione
contiene in realta' una
concentrazione 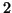 molale di particelle (ioni
molale di particelle (ioni 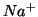 e
e
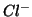 ) generate per dissociazione:
) generate per dissociazione:
- Spesso, ci si riferisce alla concentrazione totale di particelle
che determina l'entita' di una proprieta' colligativa come alla
concentrazione colligativa.
- Ovviamente, nel caso di un soluto non elettrolita (ad esempio lo
zucchero), la concentrazione colligativa coincide con quella formale.
- Se un soluto e' un elettrolita debole, cioe' non si dissocia
completamente, la concentrazione colligativa si ottiene sommando la
concentrazione del soluto indissociato a quella di tutte le particelle
generate dalla dissociazione:




Next: Slide n. 235: massa
Up: Slides delle lezioni del
Previous: Slide n. 233: la