



Next: Slide n. 142: il
Up: Slides delle lezioni del
Previous: Slide n. 140: procedura
Una teoria piu' particolareggiata del legame chimico: la teoria del
legame di valenza (VB)
- La teoria di Lewis (postulata prima dell'avvento della
meccanica quantistica) considera gli elettroni di valenza degli atomi
che formano legami, ma prescinde totalmente dal fatto che tali
elettroni sono descritti da orbitali atomici. La teoria del legame di
valenza integra il modello di Lewis nell'ambito della meccanica
quantistica, mettendo in relazione il legame fra due atomi con gli
orbitali atomici che descrivono gli elettroni implicati nel legame
stesso
- Cio' che nella teoria di Lewis e' descritto come ``condivisione''
di una coppia di elettroni, nella teoria del legame di valenza diventa
``sovrapposizione'' di opportuni orbitali atomici. La conseguenza e'
sempre la stessa: un aumento della densita' elettronica fra i nuclei dei
due atomi che si legano, con conseguente abbassamento dell'energia del
sistema
- I postulati fondamentali della teoria del legame di valenza:
- Il legame fra due atomi si realizza mediante sovrapposizione di
due opportuni orbitali atomici, uno per ciascun atomo. Nella
maggioranza dei casi, si puo' assumere che i due orbitali che si
sovrappongono per formare il cosiddetto orbitale di legame
siano semioccupati, cioe' contengano un elettrone ciascuno
- Nell'orbitale di legame che si viene a formare si vengono
cosi' a trovare due elettroni con spin antiparallelo
Esempio 50
La formazione del legame 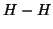 in
in 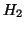 viene descritta mediante la
sovrapposizione dei due orbitali atomici
viene descritta mediante la
sovrapposizione dei due orbitali atomici 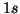 semioccupati su ciascun
atomo di idrogeno.
semioccupati su ciascun
atomo di idrogeno.




Next: Slide n. 142: il
Up: Slides delle lezioni del
Previous: Slide n. 140: procedura
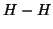 in
in 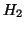 viene descritta mediante la
sovrapposizione dei due orbitali atomici
viene descritta mediante la
sovrapposizione dei due orbitali atomici 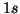 semioccupati su ciascun
atomo di idrogeno.
semioccupati su ciascun
atomo di idrogeno.