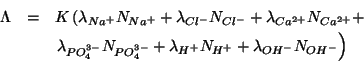Next: Slide n. 9: La
Up: Laboratorio di Chimica Analitica
Previous: Slide n. 7: La
In prima approssimazione, la conducibilita' specifica dipende
dalle concentrazioni ioniche.
-
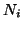
- concentrazione equivalente dello ione
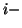 esimo
esimo
-
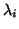
- conducibilita' ionica individuale dello ione
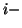 esimo
esimo
Quindi:
Esempio: soluzione acquosa contenente 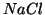 e
e
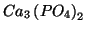 .
.
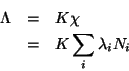
![]() e
e
![]() .
.