



Next: Slide n. 77: Cenni
Up: Slides delle lezioni del
Previous: Slide n. 75: disproporzione
Bilanciamento delle reazioni redox mediante scomposizione in semireazioni
- se la reazione e' scritta in forma molecolare, scriverla in forma ionica
- dall'analisi del numero di ossidazione degli elementi presenti,
individuare le coppie redox coinvolte nella reazione
- scrivere le semireazioni corrispondenti e per ciascuna di esse
bilanciare (in questo ordine):
- la massa dell'elemento che cambia stato di ossidazione
- gli elettroni
- le cariche (con ioni
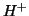 o
o 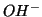 , a seconda che la reazione
avvenga in ambiente acido o basico, rispettivamente)
, a seconda che la reazione
avvenga in ambiente acido o basico, rispettivamente)
- le masse (utilizzando eventualmente molecole di acqua)
- sommare le semireazioni, moltiplicandole eventualmente per opportuni
fattori, in modo che il numero di elettroni acquistati dall'ossidante
sia uguale al numero di elettroni persi dal riducente
- semplificare i coefficienti stechiometrici delle specie eventualmente
presenti sia al primo che al secondo membro dell'equazione
- se e' richiesto di scrivere l'intera equazione in forma molecolare,
associare ad ogni specie ionica il rispettivo controione,
rispettando il bilancio di massa per le nuove specie cosi' introdotte




Next: Slide n. 77: Cenni
Up: Slides delle lezioni del
Previous: Slide n. 75: disproporzione
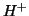 o
o 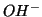 , a seconda che la reazione
avvenga in ambiente acido o basico, rispettivamente)
, a seconda che la reazione
avvenga in ambiente acido o basico, rispettivamente)