



Next: Slide n. 436: figura
Up: Slides delle lezioni del
Previous: Slide n. 434: esempio
Il processo di elettrolisi consiste in questo caso nel far avvenire la
reazione su scritta nel verso contrario a quello spontaneo, cioe':
A questo scopo bisogna forzare gli elettroni nel circuito esterno a
muoversi dalla semicella
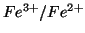 a quella
a quella
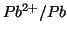 . Cio' si realizza connettendo esternamente le due
semicelle tramite un generatore di differenza di potenziale: il
connettore
. Cio' si realizza connettendo esternamente le due
semicelle tramite un generatore di differenza di potenziale: il
connettore 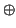 del generatore va collegato al metallo (in
questo caso potrebbe essere un filo di
del generatore va collegato al metallo (in
questo caso potrebbe essere un filo di 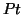 ) della semicella
) della semicella
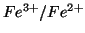 . Inoltre, il generatore dovra' produrre
una differenza di potenziale maggiore di quella dovuta ai
due potenziali elettrodici
. Inoltre, il generatore dovra' produrre
una differenza di potenziale maggiore di quella dovuta ai
due potenziali elettrodici
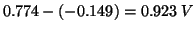 .
.