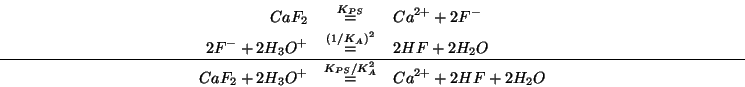Next: Slide n. 369: esempio
Up: Slides delle lezioni del
Previous: Slide n. 367: esempio
- La solubilita' di molti composti ionici e' influenzata dal
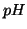 della soluzione. In generale, il
della soluzione. In generale, il 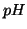 influenza la solubilita' di un
composto ionico quando uno o entrambi gli ioni che lo costituiscono
possono reagire con ioni idronio o ossidrile.
influenza la solubilita' di un
composto ionico quando uno o entrambi gli ioni che lo costituiscono
possono reagire con ioni idronio o ossidrile.
- Molti idrossidi sono poco solubili (
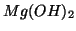 ,
, 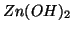 ,
,
 ). L'influenza del
). L'influenza del 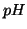 sulla solubilita' di questi
composti e' riconducibile all'effetto dello ione comune: chiaramente, per
il principio di Le Chatelier, la solubilita' di questi idrossidi
aumenta al diminuire del
sulla solubilita' di questi
composti e' riconducibile all'effetto dello ione comune: chiaramente, per
il principio di Le Chatelier, la solubilita' di questi idrossidi
aumenta al diminuire del 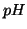 .
.
- Molti sali contengono come anione la base coniugata di un acido debole
(acetati, solfuri, carbonati, fosfati): la loro solubilita' e'
influenzata dal
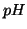 in quanto l'anione reagisce con gli ioni idronio:
in quanto l'anione reagisce con gli ioni idronio:
- In base al principio di Le Chatelier, il sale si scioglie in
misura maggiore per cercare di compensare il consumo di anione causato
dalla reazione con gli ioni idronio. In generale, dunque, la solubilita'
dei sali contenenti l'anione di un acido debole aumenta al diminuire del
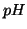 .
.