



Next: Slide n. 212: distribuzione
Up: Slides delle lezioni del
Previous: Slide n. 210: figura
- La semplice descrizione dell'equilibrio liquido vapore ora vista
spiega anche la dipendenza della pressione di vapore dalla
temperatura. Si e' visto che la velocita' di evaporazione dipende solo
dalla temperatura ed e' connessa con l'energia cinetica posseduta
dalle molecole del liquido: maggiore e' la temperatura, maggiore e'
l'energia cinetica media delle molecole e maggiore sara' il numero di
molecole che riescono ad abbandonare la superficie del liquido
nell'unita' di tempo.
- Si e' anche visto che l'equilibrio viene raggiunto quando la
velocita' di condensazione raggiunge il valore di quella di
evaporazione.
- Supponiamo che il sistema si trovi in condizioni di equilibrio a
una certa temperatura. Cosa accade se innalziamo improvvisamente la
temperatura?
- A temperatura piu' elevata, l'energia cinetica media delle
molecole nella fase liquida aumenta e di conseguenza aumenta la frazione di
molecole che, nell'unita' di tempo, passano nella fase vapore (figura): subito
dopo l'innalzamento della temperatura la velocita' di evaporazione e' quindi
maggiore della velocita' di condensazione.
- Come gia' visto, cio' comporta che la concentrazione di molecole
d'acqua nella fase vapore aumenti (perche', nell'unita' di tempo, si
ha un passaggio netto di molecole dalla fase liquida alla fase vapore)
- Un aumento della concentrazione in fase vapore porta
necessariamente ad un aumento della velocita' di condensazione
(
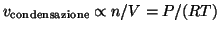 ): la velocita' di
condensazione (e la pressione) continua ad aumentare fino a che
raggiunge il valore (piu' elevato a causa dell'aumento di temperatura)
della velocita' di evaporazione. A questo punto il sistema ha
raggiunto un nuovo stato di equilibrio e la pressione del vapore e'
aumentata (figura).
): la velocita' di
condensazione (e la pressione) continua ad aumentare fino a che
raggiunge il valore (piu' elevato a causa dell'aumento di temperatura)
della velocita' di evaporazione. A questo punto il sistema ha
raggiunto un nuovo stato di equilibrio e la pressione del vapore e'
aumentata (figura).




Next: Slide n. 212: distribuzione
Up: Slides delle lezioni del
Previous: Slide n. 210: figura