



Next: Slide n. 18: definizione
Up: Slides delle lezioni del
Previous: Slide n. 16: massa
La mole
- Le reazioni chimiche coinvolgono particelle (atomi e/o molecole)
che si combinano secondo rapporti numerici definiti.
- Si pone il problema di contare le particelle coinvolte
in una reazione
- Date le dimensioni di atomi e molecole, essi non vengono contati
ad uno ad uno, ma in blocchi costituiti sempre dallo stesso numero di
particelle. Tale numero, indicato generalmente con
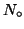 , viene
detto Numero di Avogadro.
, viene
detto Numero di Avogadro.
- Il concetto e' identico a quello secondo cui le uova, ad
esempio, vengono confezionate e vendute non singolarmente, ma in
blocchi di 6 o 12
- La quantita' di materia corrispondente ad un numero di Avogadro
di atomi o molecole (in generale di particelle) si definisce
mole (simbolo
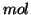 ). Ad esempio,
). Ad esempio, 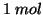 di
sodio e' la quantita' di sodio corrispondente a un numero di Avogadro
di atomi di sodio
di
sodio e' la quantita' di sodio corrispondente a un numero di Avogadro
di atomi di sodio
- Tanto per rifarci al parallelo con le uova, il concetto di mole
e' identico a quello di ``dozzina'': una dozzina di uova e' una
quantita' di uova corrispondente a
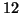 uova
uova




Next: Slide n. 18: definizione
Up: Slides delle lezioni del
Previous: Slide n. 16: massa