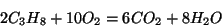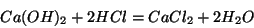Next: Slide n. 14: un
Up: Slides delle lezioni del
Previous: Slide n. 12: esempi
I punti fondamentali della teoria atomica della materia:
- La materia e' costituita da atomi
- Esistono diversi tipi di atomi, ciascuno con caratteristiche
(es. massa) proprie
- Ogni atomo e' costituito da un nucleo compatto contenente
protoni (carichi positivamente) e neutroni (elettricamente neutri),
circondato da elettroni (carichi negativamente). In un atomo neutro,
il numero dei protoni e' uguale a quello degli elettroni
- Tutti gli atomi di un dato elemento possiedono lo stesso numero
di protoni (e quindi di elettroni): tale numero e' detto numero
atomico (simbolo ``Z''). (Nella tavola periodica, tutti gli elementi
sono ordinati secondo il loro numero atomico)
- Gli atomi di un dato elemento possono differire nel numero di
neutroni contenuti nel nucleo. La somma del numero di protoni e di
quello di neutroni e' detta numero di massa (simbolo ``A'')
- Atomi aventi lo stesso numero atomico, ma diverso numero di
massa si dicono ``isotopi''. Es:
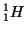 ,
, 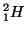 ,
, 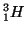
- I composti sono costituiti da molecole, cioe' aggregati di atomi
(diversi) legati fra loro in modo definito; molecole uguali sono
costituite dagli stessi atomi, nello stesso rapporto e legati nello
stesso modo (es.
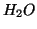 )
)
- Una reazione chimica consiste nel riarrangiamento (rottura e/o
formazione di legami) degli atomi in uno o piu' composti messi a
contatto sotto opportune condizioni
- Nelle reazioni chimiche la massa viene conservata




Next: Slide n. 14: un
Up: Slides delle lezioni del
Previous: Slide n. 12: esempi